| Переглянути всі підручники | |||||||||||||
| << | < | 33 | 34 | 35 | 36 | 37 | 38 | 39 | 40 | 41 | 42 | > | >> |
§ 6. СУЛЬФАТНА КИСЛОТА
Сульфатна кислота H2S04 (безводна, 100%-ва) — важка безбарвна оліїста рідина.
Сульфатна кислота —їдка рідина, тому треба остерігатись, щоб вона не потрапила на шкіру й одяг. А якщо це сталося, треба швидко змити її великою кількістю води, після чого нейтралізувати розчином соди і знову змити водою.
Пам'ятайте таке правило:
не можна воду доливати до концентрованої сульфатної кислоти! Для розбавляння кислоту треба доливати до води невеликими порціями.
Хімічні властивості сульфатної кислоти багато в чому залежать від її концентрації. В лабораторіях та промисловості використовують розбавлену і концентровану сульфатну кислоту, хоча такий поділ дещо умовний.
Розбавлена сульфатна кислота виявляє всі хімічні властивості, характерні для кислот.
1. Зміна кольору індикатора. Пригадайте, якого кольору набувають відомі вам індикатори в кислому середовищі.
2. Дисоціація кислоти. Сульфатна кислота двохосновна, належить до сильних кислот. У водних розчинах вона дисоціює на йони за двома ступенями (за першим — практично повністю):
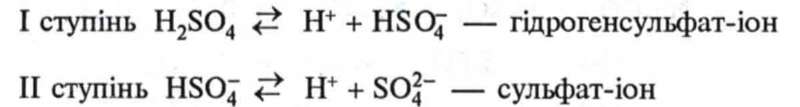
Ось чому в процесі нейтралізації розчинів сульфатної кислоти H2S04 утворюються два ряди солей: середні солі — сульфати і кислі солі —гідрогенсульфати.
3. Взаємодія з основами. Якщо у пробірку з розбавленою сульфатною кислотою добавити дві-три краплі фіолетового
| Переглянути всі підручники | |||||||||||||
| << | < | 33 | 34 | 35 | 36 | 37 | 38 | 39 | 40 | 41 | 42 | > | >> |