| Переглянути всі підручники | |||||||||||||
| << | < | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | > | >> |
спостерігається свічення полум'я. Пригадайте, що метан горить майже безбарвним полум'ям.
Пояснити цю відмінність можна, виходячи зі складу молекул метану й етилену. Масова частка Кароону в метані становить 75 %, а з етилені— 86 %.
Отже, етилен, розкладаючись у полум'ї, утворює порівняно з метаном більше частинок вуглецю, що розжарюються і зумовлюють свічення. У верхній частині полум'я вони згоряють до вуглекислого газу.
Можна припустити, що ацетилен горітиме ще яскравішим полум'ям, оскільки масова частка Карбону в його молекулі становить 92 %. Переконаємось у цьому на досліді (мал. 23). Справді, ацетилен горить кіптявим полум'ям.
Для повного згоряння ацетилену, наприклад при ацетиленовому зварюванні металів, у полум'я додатково подається повітря або кисень.
Нснасичений характер карбон-карбо-нових зв'язків зумовлює характерні хімічні властивості етилену й ацетилену.
З'ясовуючи хімічну активність насичених вуглеводнів, ми проводили випробування розчином перманганату калію: його забарвлення не змінювалося. Нена-сичсні вуглеводні етилен і ацетилен виявляють значну активність у цій реакції: фіолетове забарвлення розчину зникає під час пропускання крізь нього цих газів. Отже, етилен і ацетилен вступають у реакцію часткового окиснення з перманганатом калію. Внаслідок реакції утворюються продукти складної будови.
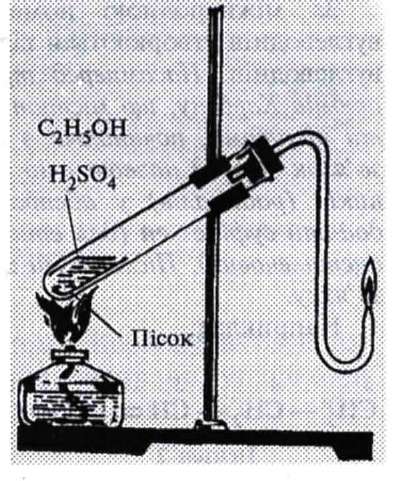
Мал. 22. Добування етилену в лабораторії
 |
|
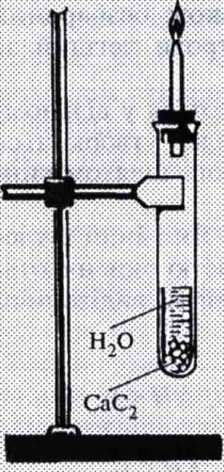
Мал. 23. Добування ацетилену в лабораторії |
| Переглянути всі підручники | |||||||||||||
| << | < | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | > | >> |