| Переглянути всі підручники | |||||||||||||
| << | < | 53 | 54 | 55 | 56 | 57 | 58 | 59 | 60 | 61 | 62 | > | >> |
Будова молекули. Молекула аміаку NH3 являє собою диполь: спільні електронні пари дуже зміщені до атома Нітрогену (чому?):
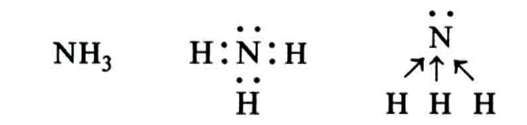 |
|
• Зазначте електронні формули атомів Нітрогену і Гідрогену, покажіть графічно розміщення електронів по орбіталях і поясніть, якими електронами утворюється ковалентний зв'язок у молекулі аміаку і чому він полярний. Яка валентність і ступінь окиснення Нітрогену в аміаку? |
Фізичні властивості. Аміак NH3 — безбарвний газ, а різким запахом, набагато легший за повітря, дуже добре розчиняється у воді (за 20°С в 1 об'ємі води — 700 об'ємів NH3), за температури, нижчій за -33,4 °С переходить у рідкий стан. Дуже уражує слизові оболонки очей і дихальних шляхів.
Хімічні властивості. Для аміаку характерні реакції окиснення і приєднання.
 |
|
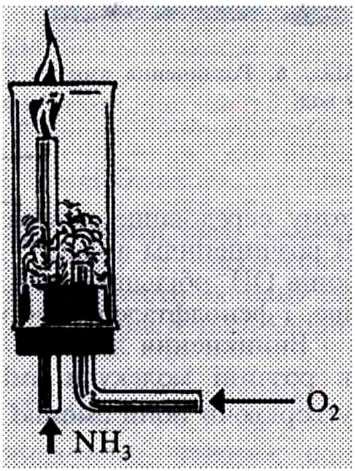
Мал. 5. Горіння аміаку |
1. Окиснення аміаку. Аміак, маючи низький ступінь окиснення Нітрогену -3, поводить себе як відновник. Відновні властивості аміаку виявляються під час горіння його в кисні (мал. 5).
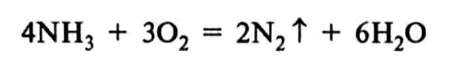
За наявності каталізатора (Pt) реакція окиснення аміаку змінюється: замість вільного азоту утворюється оксид нітрогену(ІІ) N0:
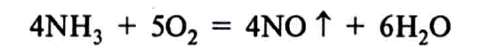
| Переглянути всі підручники | |||||||||||||
| << | < | 53 | 54 | 55 | 56 | 57 | 58 | 59 | 60 | 61 | 62 | > | >> |