| Переглянути всі підручники | |||||||||||||
| << | < | 54 | 55 | 56 | 57 | 58 | 59 | 60 | 61 | 62 | 63 | > | >> |
• Складіть для наведених рівнянь електронний баланс, обґрунтуйте розстановку коефіцієнтів і доведіть, що аміак в обох випадках —відновник.
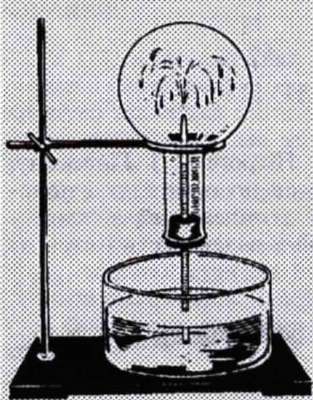
2. Взаємодія з водою. Аміак добре розчиняється у воді, утворюючи аміачну воду. Висока розчинність аміаку пояснюється тим, що він реагує з водою. Якщо суху колбу, заповнену аміаком і закриту пробкою зі вставленою трубкою з відтягнутим кінцем, занурити у воду, до якої додано кілька крапель розчину фенолфталеїну, то з безбарвної рідини починає бити малиновий «фонтан» (мал. 6). Забарвлення аміачної води свідчить про те, що водний розчин аміаку має лужну реакцію.
Як це можна пояснити? У воді концентрації йонів однакові:
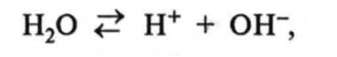
тому середовище нейтральне, і фенолфталеїн безбарвний. З розчиненням аміаку NH3 у воді концентрація гідроксид-іонів ОН" збільшується, отже, утворюється лужне середовище, і фенолфталеїн стає малиновим.
Виникнення лужного середовища пояснюється тим, що в розчині молекули аміаку приєднують йони Гідрогену,
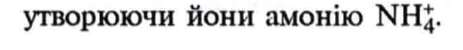
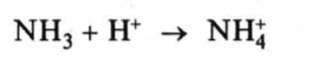
При цьому вивільнюються з води гідроксид-іони ОН , що й надає розчину лужної реакції.
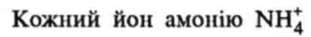
має чотири ковалентні зв'язки. Три з них утворюються за рахунок трьох неспарених електронів, які є на р-орбіталях зовнішнього електронного шару атома Нітрогену. Четвертий зв'язок утворюється за донорно-акценторним механізмом між атомом Нітрогену аміаку (донор) та йоном Гідрогену (акцептор):
| Переглянути всі підручники | |||||||||||||
| << | < | 54 | 55 | 56 | 57 | 58 | 59 | 60 | 61 | 62 | 63 | > | >> |