| Переглянути всі підручники | |||||||||||||
| << | < | 59 | 60 | 61 | 62 | 63 | 64 | 65 | 66 | 67 | 68 | > | >> |
Лабораторна робота 4 Утворення солей амонію
До отвору пробірки з концентрованим розчином аміаку піднесіть скляну паличку, змочену концентрованою хлоридною кислотою.
Як пояснити утворення диму? Дослід повторіть, узявши замість хлоридної концентровану нітратну кислоту. Напишіть рівняння проведених реакцій.
Застосування. Нітрат амонію NH4N03 і сульфат амонію (NH4)2S04 використовують головним чином як добрива. Нітрат амонію NH4N03 (в суміші з алюмінієм і вугіллям) застосовують для виготовлення вибухової речовини —амоналу. Хлорид амонію NH4C1 під назвою «нашатир» використовують у процесі паяння для очищення поверхні паяльника.
Коли нагрітий паяльник занурюють у нашатир NH4C1, то сіль розкладається (див. вище). Утворений хлороводень HC1 взаємодіє з оксидом ку-пруму(ІІ) CuO, що вкриває поверхню паяльника, внаслідок чого з'являється хлорид купруму(ІІ) CuClj, який сплавляється з надлишком нашатирю NH4C1. В результаті поверхня паяльника звільняється від оксидів, і розплавлене олово прилипає до очищеної міді.
77. Які солі називають солями амонію? Напишіть рівняння реакцій, що для них характерні. Зазначте специфічні властивості.
78. Напишіть рівняння взаємодії аміаку з сульфатною кислотою. Зважте на тс, що можуть утворитися як середня, так і кисла солі амонію. Поясніть, від чого цс залежить.
79. Карбонат амонію (NH4)2C03 застосовують у кондитерській справі як розпушувач тіста. На якій властивості солі ґрунтується такс її застосуваїпія? Відповідь проілюструйте рівнянням реакції.
80. Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення:
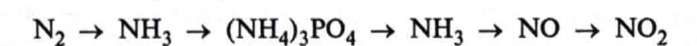 |
|
81. На сульфат амонію масою 33 г подіяли розчином лугу. При цьому виділився аміак об'ємом (н. у.) (а) 11,2 л; (в) 33,6 л; (б) 22,4 л; (г) 44,8 л. |
| Переглянути всі підручники | |||||||||||||
| << | < | 59 | 60 | 61 | 62 | 63 | 64 | 65 | 66 | 67 | 68 | > | >> |