| Переглянути всі підручники | |||||||||||||
| << | < | 66 | 67 | 68 | 69 | 70 | 71 | 72 | 73 | 74 | 75 | > | >> |
фосфатна кислота середньої сили, але нелетка. Взаємодія нітратної та фосфатної кислот з солями відбувається за умови, що береться сіль слабкішої або леткішої кислоти:
Під час нагрівання фосфатної кислоти з неї виділяється вода й утворюється дифосфатна кислота:
2Н3Р04 = Н20 + Н4Р207
6. Взаємодія з металами. Нітратна кислота реагує з металами інакше, ніж інші кислоти. Це пояснюється тим, що нітратна кислота —сильний окисник. Вона окиснює майже всі метали (за винятком золота, платини та деяких інших), перетворюючи їх на солі—нітрати. При цьому водень не виділяється, бо відновлюється Нітроген, а не Гідроген. Нітроген відновлюється тим повніше, чим активніший метал і чим розбавленіша кислота. Отже, продукти відновлення нітратної кислоти можуть бути різні. Проте концентрована кислота відновлюється, як правило, до N02 в разі взаємодії з важкими металами.
Якщо на дно колби опустити обрізки мідного дроту і долити до них концентрованої нітратної кислоти (у витяжній шафі), то одразу ж почне виділятися бурий газ N02, а розчин забарвиться у синій колір:
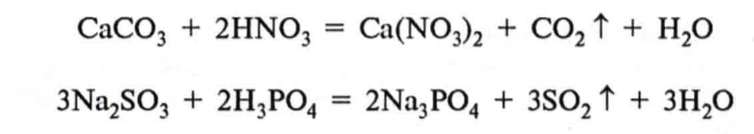 |
|
5. Термічний розклад. Нітратна кислота під час нагрівання (і під впливом світла) розкладається з виділенням бурого газу N02, через що у процесі зберігання поступово жовтіє: |
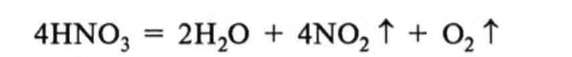
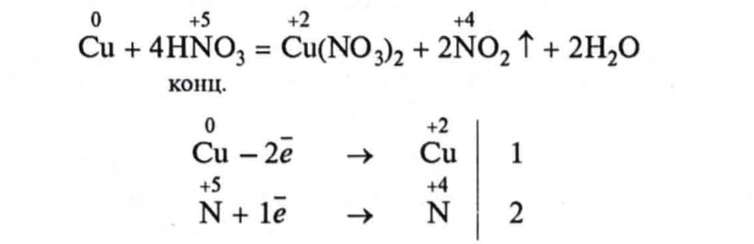
| Переглянути всі підручники | |||||||||||||
| << | < | 66 | 67 | 68 | 69 | 70 | 71 | 72 | 73 | 74 | 75 | > | >> |