| Переглянути всі підручники | |||||||||||||
| << | < | 82 | 83 | 84 | 85 | 86 | 87 | 88 | 89 | 90 | 91 | > | >> |
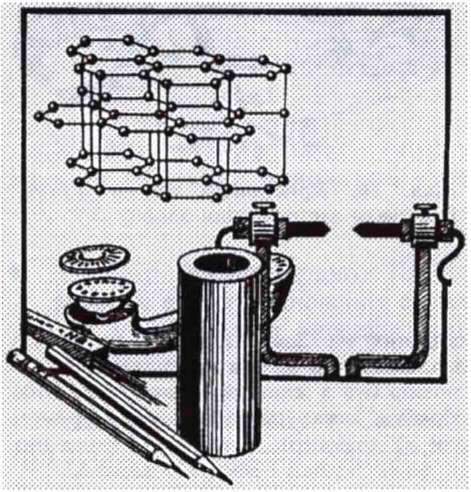
ніш блиском. Структура графіту шарувата (мал. 11): атоми Карбону розміщені шарами, що складаються з шестичленних кілець. У межах одного шару кожний атом Карбону утворює три хімічні зв'язки з трьома сусідніми атомами. Усі атоми Карбону об'єднуються у макромолекули, які являють собою нескінченні шари із шестичленних кілець.
За рахунок четвертих електронів зовнішнього електронного шару кожного атома Карбону, що не беруть участі в утворенні хімічних зв'язків у площині, виникає загальна система хімічного зв'язку, делокалізованого у межах всієї макромолекули. Цим саме і визначається електрична провідність графіту, темно-сірий колір і металічний блиск.
Шари атомів Карбону об'єднуються у кристалічні ґратки за рахунок міжмолекулярних сил.
Всередині шару графіту зв'язки між атомами ковалентно-металічні, доволі міцні, а між шарами діють міжмолекулярні сили, доволі слабкі. Тому графіт легко розшаровується на лусочки. Це робить кристали графіту неміцними, а сам мінерал м'яким. Навіть під час слабкого тертя графіту по паперу на ньому залишається сірий слід. Графіт тугоплавкий (tпл. = 3800 °С), хімічно дуже стійкий. З нього виготовляють вогнетривкі тиглі, мастила, синтетичні алмази, електроди, обкладки для електролітичних ванн, труби теплообмінників (див. мал. 11). В ядерних реакторах графіт використовують як уповільнювач нейтронів. З графіту роблять грифелі для олівців.
У промисловості, крім природного, використовують штучний графіт. Його добувають з кращих сортів кам'яного вугілля (кокс, антрацит). Процес відбувається в електропечах за температури 2600—3000 °С і тиску 250 МПа без доступу повітря.
 |
|
Мел. 11. Кристалічні ґратки графіту. Приклади застосування графіту |
| Переглянути всі підручники | |||||||||||||
| << | < | 82 | 83 | 84 | 85 | 86 | 87 | 88 | 89 | 90 | 91 | > | >> |